A tabela periódica é um dos maiores ícones da ciência. Com seus 118 elementos organizados de maneira meticulosa, ela não é apenas uma ferramenta visualmente impressionante, mas também um recurso fundamental para cientistas em todo o mundo. Sua estrutura ordenada por número atômico e propriedades químicas oferece insights profundos sobre os blocos fundamentais da matéria. Vamos explorar como essa obra-prima científica foi criada, sua evolução ao longo do tempo e as aplicações práticas que ela tem hoje.
Quem criou a tabela periódica?

A invenção da tabela periódica remonta ao trabalho do químico russo Dmitri Mendeleev, frequentemente chamado de o “pai” da tabela periódica. Durante a década de 1860, enquanto trabalhava no livro “Princípios de Química”, Mendeleev enfrentou o desafio de organizar os 63 elementos conhecidos na época. Ele escrevia as propriedades dos elementos em cartas individuais e as organizava conforme seus pesos atômicos. Ao fazer isso, percebeu padrões que revelaram uma relação entre peso atômico e propriedades químicas.
Mendeleev foi além: ele previu a existência de elementos ainda não descobertos e suas propriedades. Por exemplo, ele sugeriu a existência do “eka-alumínio”, que anos depois foi identificado como gálio, com propriedades incrivelmente similares às suas previsões.
A estrutura da tabela periódica
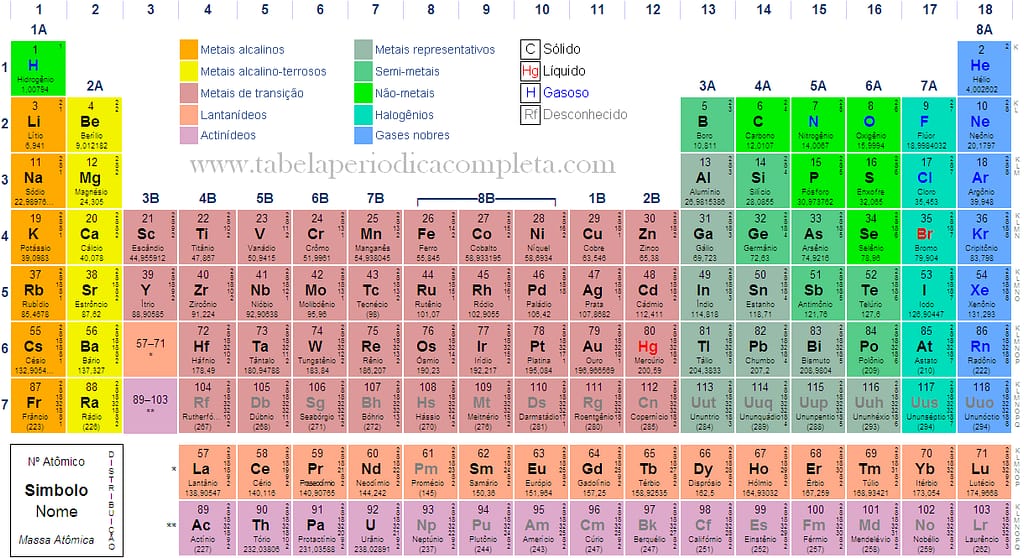
A tabela periódica atual está organizada em sete linhas horizontais (períodos) e 18 colunas verticais (grupos). A posição de cada elemento reflete o número de prótons em seu núcleo (número atômico) e o comportamento químico.
- Número atômico: Indica a quantidade de prótons no núcleo do átomo. Por exemplo, o carbono tem 6 prótons, enquanto o oxigênio tem 8.
- Símbolo atômico: É a abreviação do nome do elemento. Alguns símbolos derivam do latim, como “Au” para ouro (“aurum”).
- Massa atômica: Representa a média ponderada das massas dos isótopos de um elemento.
Evolução da tabela periódica
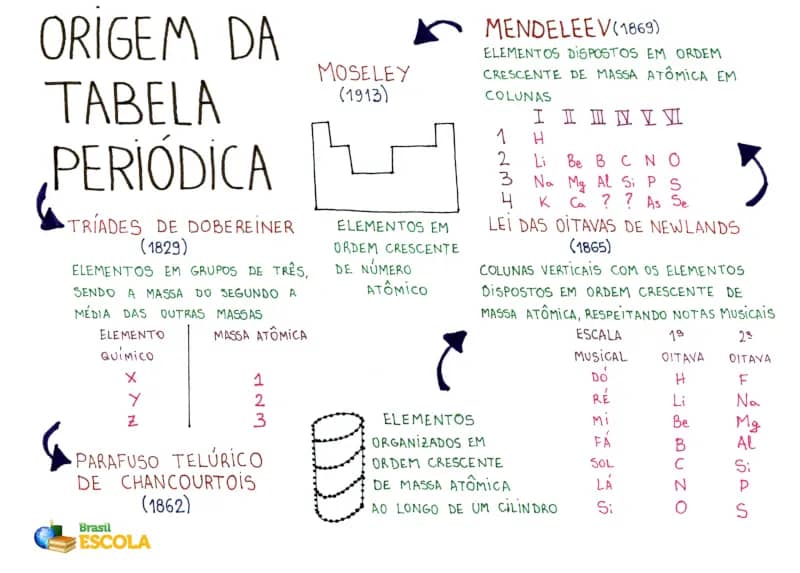
Desde sua criação, a tabela periódica cresceu significativamente. Quando Mendeleev a publicou pela primeira vez, em 1869, ela continha apenas 63 elementos. Hoje, inclui 118 elementos, com os mais recentes sendo sintetizados em laboratórios. Esses elementos superpesados, como o oganêssônio (Og), são altamente instáveis, existindo por apenas frações de segundo antes de se desintegrarem.
Os avanços tecnológicos, como aceleradores de partículas, permitiram a criação de novos elementos, estendendo os limites da tabela. Contudo, ainda é um mistério até onde ela pode ser expandida.
Como a tabela periódica é usada hoje?

Mais de um século após sua criação, a tabela periódica continua sendo uma ferramenta indispensável. Ela guia pesquisas em química, física e engenharia, permitindo a previsão de como elementos interagem. Exemplos de aplicações incluem:
- Indústria eletrônica: Elementos dos grupos III e V, como o gálio e o índio, são usados em semicondutores.
- Saúde: O magnésio é utilizado em ligas biodegradáveis para implantes ósseos.
- Química industrial: Gases nobres como o hélio e o neônio têm aplicações em iluminação e soldagem.
Um legado em constante expansão
A tabela periódica não é apenas uma lista; é um testemunho do engenho humano. Ela reflete nossa compreensão do universo e continua a evoluir com cada descoberta. Sua beleza está na simplicidade com que organiza o complexo, fornecendo a cientistas e estudantes uma janela para o mundo dos átomos e suas interações.
Enquanto novas fronteiras químicas são exploradas, a tabela periódica permanece como um pilar fundamental da ciência. Afinal, entender os elementos é compreender o próprio universo.